肝がんとは?
肝臓は右上腹部に位置し、成人で約800~1,400gの重量を持つ人間の体内で脳に次いで二番目に大きな臓器です。肝臓の血流には、主に栄養を運ぶ役割をもつ門脈と、酸素を運ぶ肝動脈があり、約70~80%が門脈から、残りが肝動脈から供給され、肝静脈に集まって心臓に戻ります。
門脈は主に腸からの血流を集める血管です。小腸で吸収された栄養素は、この門脈を通って肝臓に運び込まれます。腸で吸収されて運ばれたさまざまな物質の、代謝、排泄、解毒など生命の維持に必要な多くの働きを肝臓は行なっています。また消化液である胆汁を作り、胆管を通って十二指腸から腸管に流れ、消化の役割も担っています。
肝癌とは、肝臓の中にできたがんのことです。統計学的には我が国では年間約30,000人が肝がんで亡くなっています。肝癌は原発性肝癌と転移性肝癌に分類され、さらに前者は、肝実質を構成する肝細胞が癌化する肝細胞癌と、肝内を走行する胆管上皮細胞が癌になる胆管細胞癌から構成されます。一方後者は、他の臓器にできた癌(大腸癌など)が、治療前・治療後に関わらず肝臓に転移して腫瘍形成しているもの(転移性肝腫瘍)を指します。

危険因子
日本の肝細胞癌の患者さんの多くはB型肝炎ウイルスやC型肝炎ウイルスの持続感染が原因です。肝炎ウイルスに感染してから慢性肝炎、あるいは肝硬変の状態で肝細胞癌が発生します。B型肝炎ウイルス、C型肝炎ウイルスの感染は母子感染、昔の輸血、予防注射の針や注射器の使い回し、針刺し行為、鍼治療、刺青などが原因でおこります。近年、薬物治療の進歩によりウイルスが排除されるようになってまいりましたが、慢性肝炎の時期の肝障害は依然発癌リスクをかかえており、定期検査が必要です。その他の肝細胞癌の発生原因としては、飲酒によるアルコール性肝硬変、また糖尿病や高血圧などの基礎疾患を背景とする非アルコール性脂肪肝炎などがあり、とくに後者は近年増加しています。これらの危険因子を有する方は、まず食生活で節制を心掛けたうえで、何も症状がなくても定期的な血液検査や肝臓エコー検査などを受ける機会をつくることをお勧めします。
肝内胆管癌の発生に関わる危険因子としては、同様に、肝硬変、B型肝炎、C型肝炎、飲酒、糖尿病、肥満、喫煙、非アルコール性脂肪肝が挙げられるほか、肝吸虫や原発性硬化性胆管炎や肝内結石症、先天性胆道拡張症、カロリー病、炎症性腸疾患、特定の化学物質への曝露も指摘されている。
発見のための検査
上記発癌危険因子を持つ方は特に、以下のような検査を定期的に受けることが必要です。肝臓は大きな臓器であり、通常発癌初期には自覚症状がないため、症状がないから大丈夫なわけではありません。
血液検査
AST/ALT
肝細胞が壊されると血液の中に流れ出してくる酵素です。肝炎の程度を知る検査です。
血小板
血が固まる時に必要とされる血球成分です。進行した慢性肝炎や肝硬変になると血液の中の血小板数が減ってきます。C型肝炎では10万/mm3以下に低下すると肝がんの発生の危険性が高くなります。
アルブミン
肝臓で作られる蛋白の一部です。肝機能が悪くなると低下し、むくみや腹水がでてきます。
総ビリルビン
肝細胞が障害されたときに上がってきます。血液中の総ビリルビンが増えると黄疸がでます。
AFP
肝細胞癌担癌状態で上昇する可能性のある腫瘍マーカーです。
PIVKA-Ⅱ
肝細胞癌担癌状態で上昇する可能性のある腫瘍マーカーです。ただし、ビタミンK欠乏をおこす抗凝固剤(ワーファリン)などを服用しているときは肝細胞癌でなくても上昇することがあります。
CA19-9
胆管細胞癌で上昇する可能性のある腫瘍マーカーです。
画像検査
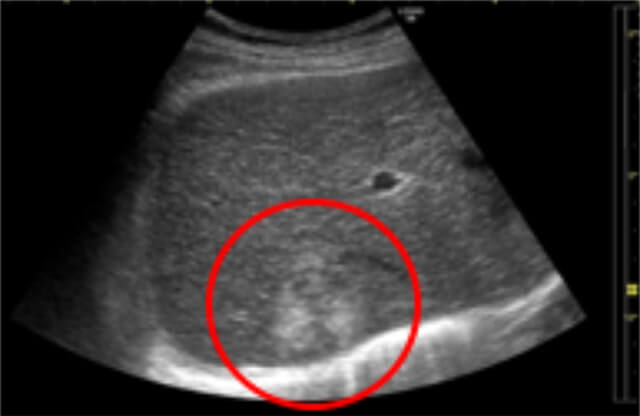
超音波検査(エコー)
超音波を利用して体の内部を観察する検査です。肝臓の状態(脂肪肝、慢性肝炎、肝硬変など)を観察し、肝の内部の腫瘍をみつけることができます。進行した慢性肝炎や肝硬変では3ヵ月毎に検査することが推奨されています。
エコー画像
CT検査
X線を用いた検査で、造影剤を使用して撮影します。超音波で見えにくい部分でも見ることができます。肝細胞がんは肝動脈からの血液で栄養されるため、造影剤を用いることによって癌が見つけやすくなります。
CT画像

EOB-MRI検査
磁場を使って撮影する検査です。エックス線の被曝がなく、いろいろな方向から撮影ができます。CTと原理が違うためCTで分かり難い腫瘍がはっきり見えることもあります。MRIにもMRI用の造影剤があり、造影剤を用いることによりさらに腫瘍は見つけやすくなります。
FDG-PET/CT検査
放射性同位元素をつけた薬剤を投与して、体内で、悪性腫瘍などの糖代謝が活発に行われる場所に異常集積する部位をCT検査で高精度に診断する検査です。生理的集積との区別が必要な一方で、リンパ節転移など、遠隔転移の有無をスクリーニングする上で有用な場合があります。
MRI画像

PET-CT画像

病期:ステージ
原発性肝癌の進行度分類はⅠ、Ⅱ、Ⅲ、Ⅳの4段階あり、数字が大きいほどがんが進行していることを意味します。以下に「原発性肝癌取り扱い規約(第6版)」から抜粋したものを示します。
- 1個だけである
- 直径2cm以下である
- 血管や胆管への浸潤がない
| ステージ | 条件の合致性 |
|---|---|
| Ⅰ期 | 1)、2)、3)のすべてに合致する |
| Ⅱ期 | 1)、2)、3)の2項目に合致する |
| Ⅲ期 | 1)、2)、3)の1項目に合致する |
| Ⅳ期 | 1)、2)、3)のすべてに合致しない さらに、リンパ節転移や遠隔転移(肝臓の外の身体部分に転移がある)のある場合は、それだけでステージⅣとなります。 |
転移性肝癌は、癌原発臓器の癌細胞が血流にのって遠隔臓器である肝臓に生着し腫瘤形成している状態であり、進行度は通常IVに分類されます。
治療法
肝切除(手術)
最大の利点は、がんを完全に取り除く最も確実な方法です。欠点は、身体に傷をつけ、合併症も少なからずあり、手術に起因する死亡が約3%あること、標準的には2週間の入院とその後数週間の自宅療養が必要であること、手術前と同じ社会活動(ゴルフ、テニスなどのスポーツも含めて)に戻るには1-2か月かかることなどです。
肝切除の対象となるには、いくつかの条件があります。体力的に日常生活のすべてを他人の介助なしにできる体力のあること、肝機能的には強い自覚症状がなく腹に水がたまる(腹水)ことや黄疸がないことなどです。これらを「機能的条件」といい、これにより肝臓の何%まで切除可能かが決まります。もうひとつがんの大きさ、数、分布状態などを「解剖学的条件」といい、これによりがんを取り除くためには肝臓の何%を切除する必要があるかが決まります。先の「機能的条件」からみた切除可能範囲(%)が、「解剖学的条件」からみた切除必要範囲(%)より大きければはじめて切除可能となります。
したがって、直径2~3cm程度の小さながんで1個だけでも、肝臓の中での位置や肝機能の程度で、手術不能ということもあります。特に肝細胞癌では慢性肝炎や肝硬変を合併している例が多く、「機能的条件」が不良のことがしばしばあります。このため、手術を考える際には、当院での再度の精密検査がしばしば必要になります。
近年、腹腔鏡下肝切除術を積極的に取り入れて施行しています。従来の開腹手術よりも創の大きさが小さいため、術後の体力の回復が早くなることが期待されます。また腹腔鏡手術特有の、拡大視効果や気腹圧による止血効果、さらに肝門部から見上げるような視野で行うことによる手術のやりやすさがあり、その適応は広がっています。さらにはロボット支援下肝切除手術も導入され、腹腔鏡下手術のメリットを生かしながらより精緻な手術が行えるようになってきました。これら低侵襲手術の適応は厳密に判断する必要がありますが、安全に行える治療として今後も広がっていくと考えています。




ラジオ波焼灼療法(RFA)
主に腫瘍が被膜に包まれている、肝細胞癌の治療選択肢のひとつです。皮膚に局所麻酔を行って、腹部エコーで腫瘍を観察しながら治療専用の針を用いてがんもしくはその周囲に針を刺入し、電流を流して熱を発生させてがんを焼灼する治療です。全身麻酔下に、開腹下、あるいは腹腔鏡で観察しながら肝臓の表面に穿刺しておこなう場合もあります。身体に与えるダメージが少なく、短期間で社会復帰できるという利点がありますが、径の大きい病変や、主要血管に近接した病変ではがんの一部が焼け残り、再発する可能性が高まる懸念があります。
肝動脈化学塞栓術(TACE)
主に動脈性の血流が豊富な肝細胞癌の治療選択肢のひとつです。手足の動脈に局所麻酔下にカテーテルを挿入し、レントゲン透視下にカテーテルを肝臓内のがんを栄養している動脈まで進めたうえで、先端から抗がん剤を流し、さらにその動脈を詰め、がん細胞を壊死させる治療法です。1回の治療に要する入院期間は1週間程度と短く、副作用としては腹痛・吐き気・食欲不振・発熱などがありますが、数日から数週でおさまります。ただし、完全に治ってしまう確率はあまり高くありませんので、数ヶ月おきに繰り返し行うことが多い治療法です。
抗がん剤治療
様々な理由で手術を含めた上記治療のよい適応でない場合、抗がん剤治療の選択を検討します。肝細胞癌においても、肝内胆管癌においても、近年効果が期待できる薬剤の開発が進んでおり、選択する機会が増えています。消化器内科と連携して治療適応を確認します。
これらの治療選択肢から、患者様ひとりひとりの状況に適した治療を行うべく、院内の消化器内科肝臓グループ、放射線科と日常的に連携し、定期的に肝癌キャンサーボードを開催して診断の確認、治療方針の検討、再治療時の方針検討を行っております。

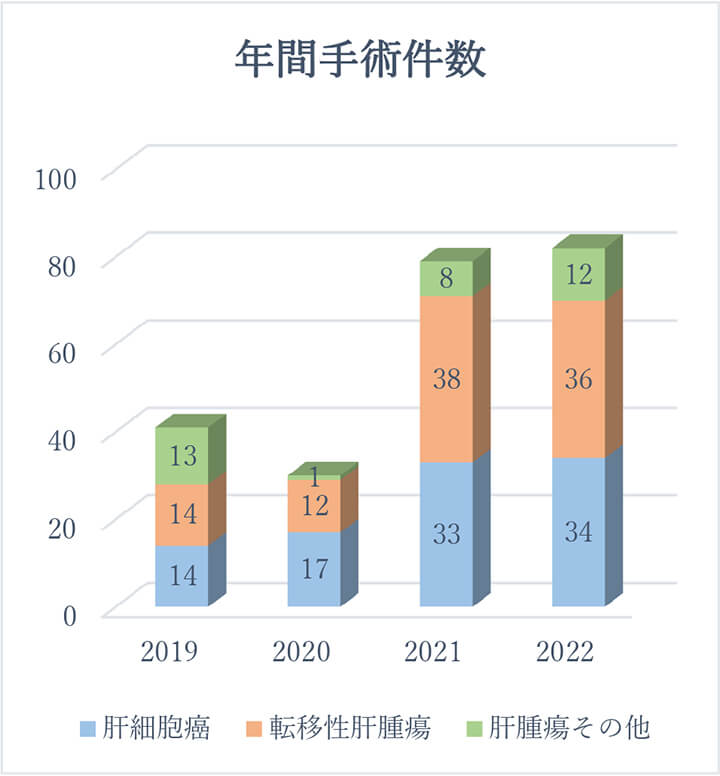
肝腫瘍手術件数の推移
疾患別
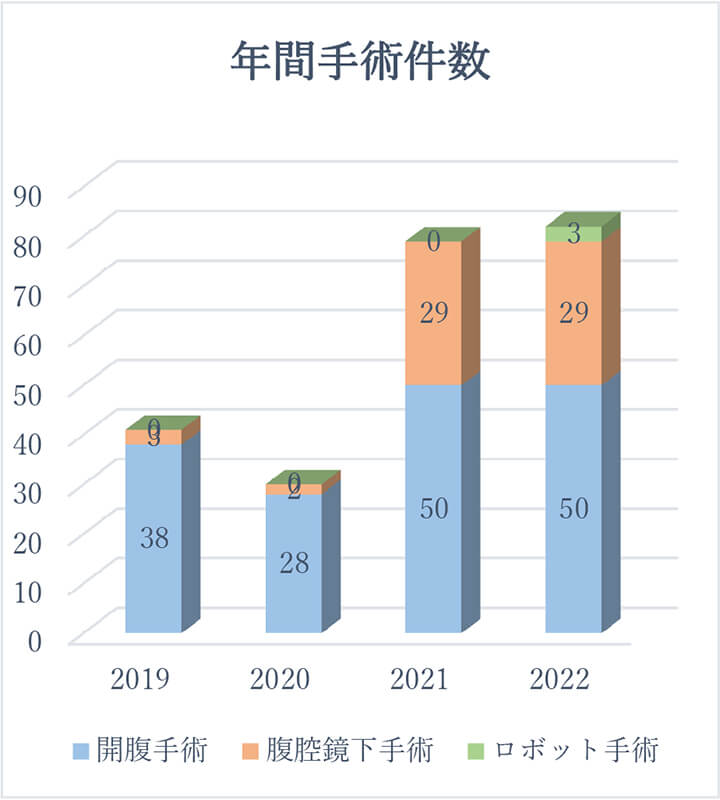
術式別
開腹移行症例
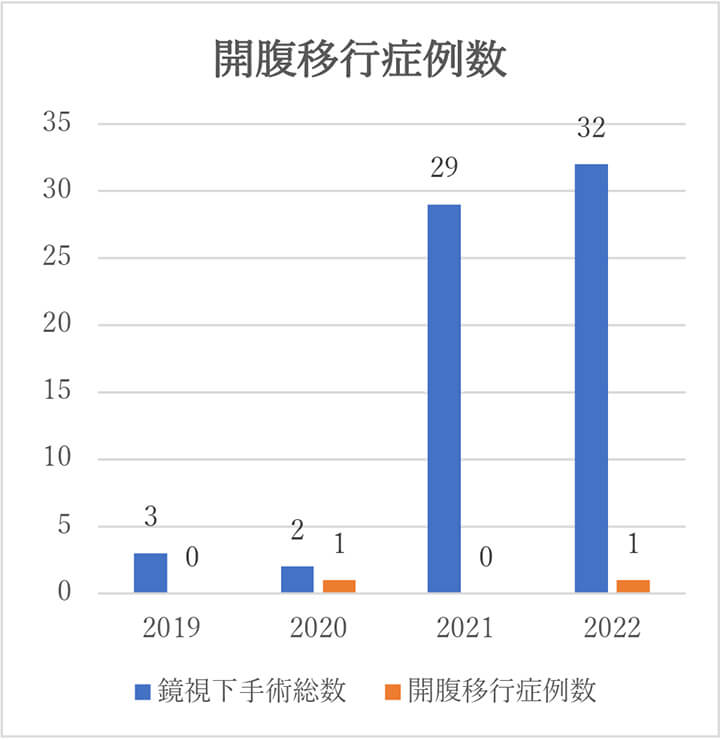
術後30日以内の死亡症例
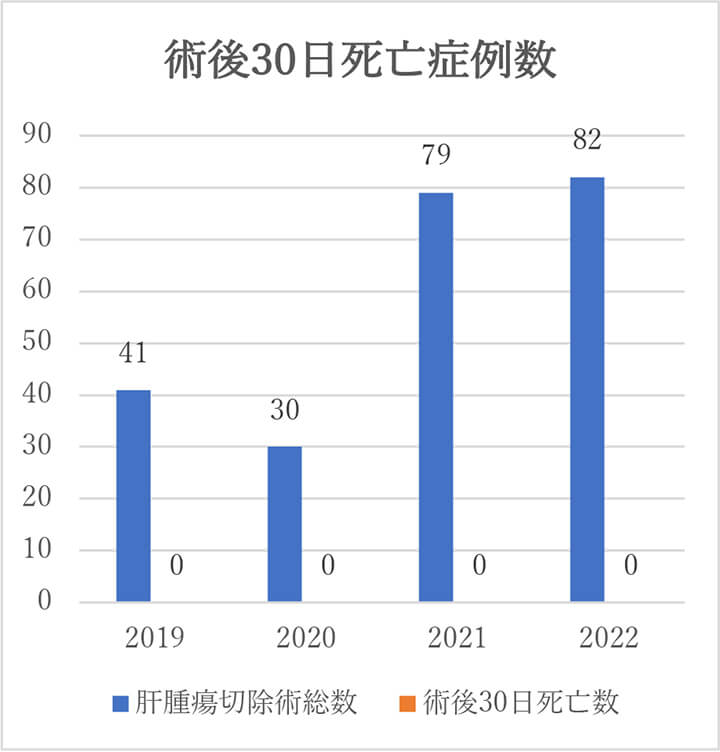
臨床試験
肝臓外科・内科領域で全国で展開されている各種臨床試験につき、積極的に参加しています。以下、一例を示します。
-
FGFR2遺伝子再構成を伴う進行性胆管癌患者に対する一次化学療法のフチバチニブ療法とゲムシタビン+シスプラチン療法を比較する第III相非盲検ランダム化試験
肝内胆管癌の術後再発症例、あるいは、局所進行や遠隔転移のために切除不能とされた症例を対象にして、FGFR2遺伝子異常の陽性者に対しフチバニチブ療法あるいはゲムシタビン+シスプラチン療法を行う臨床試験です。
手術手技の探求
-
Mizuno T et al. Ann Surg Oncol. 2017 Apr;24(4):1046-1047.
腹腔鏡下肝切除におけるGlissonean pedicle transection methodおよびICG蛍光法は正確な解剖学的切除を可能にする。

基礎研究
遺伝子マーカーを用いた肝切除後予後予測
-
Okamura Y et al. Cancer Lett. 2011 Dec 22;312(2):150-7.
肝癌組織と背景肝組織から抽出した核酸を、発現アレイ、メチル化アレイ、SNP解析アレイに提出し、癌部でメチル化によって有意に発現低下する遺伝子を同定し、発癌機序に関与する候補遺伝子としてbleomycin hydrolase (BLMH) 遺伝子を同定した。
-
Sonohara F et al. Sci Rep. 2017 Nov 23;7(1):16142.
Non-coding RNAマーカーであるHULCおよびMALAT1がC型肝炎症例の肝癌切除後の有意な予後予測マーカーとして同定された。
-
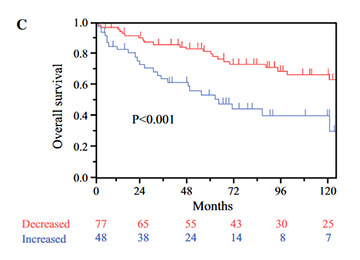
Hayashi M et al. Ann Surg Oncol. 2021 Jun;28(6):3416-3426.
肝癌細胞株における実験で、micro RNA-23b-3p発現を阻害することで肝癌増殖が抑制されることを確認した。また、肝細胞癌組織内のmicro RNA-23b-3p高発現症例(Increased)は、低発現症例(Decreased)と比較して術後生存期間が有意に不良因子であった。

術前血清マーカーを用いた肝切除後予後予測
-
Sonohara F et al. Hepatol Res. 2019 Nov;49(11):1305-1315.
肝細胞癌症例における術前血清マーカーとして、aspartate transaminase-to-platelet ratio index (APRI)が背景肝の線維化によく相関し、platelet-albumin-bilirubin (PALBI) gradeが手術時間、出血量によく相関した。
-
Hayashi M et al. Nutr Cancer. 2021;73(6):996-1003.
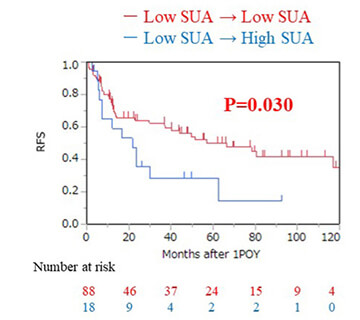
肝細胞癌と診断され切除術を受けた人の中で、術前血清尿酸値6.1mg/dl以上(High SUA)だと6.1mg/dl未満(Low SUA)の場合に比べて有意に術後再発率が高かった。また術後1年目までに血清尿酸値が6.1ml/dl以上に上昇した人(Low SUA→High SUA)も、やはり有意に術後再発率が高かった。